PRZEDRUK, oryginał dostępny pod adresem www
Tytuł oryginalny: Nomenklatura systematyczna związków organicznych
Rekomendacje IUPAC 2004
Autor: dr Marek Żylewski
Uniwersytet Jagielloński (www)
Wydział Farmaceutyczny Collegium Medicum (www)
Katedra Chemii Organicznej (www)
Kierownik: Prof. UJ, dr hab. Marek Cegła
Adres:
ul. Medyczna 9
30-688 Kraków
Kontakt: tel. 012 620 55 00
Zasady generalne
1. Mnożniki (liczebniki)
Służą do opisania liczebności podstawników, grup funkcyjnych itd. Umieszczane są zawsze przed częścią nazwy, której dotyczą
Tabela 1. Nazwy mnożników (tab 1.4)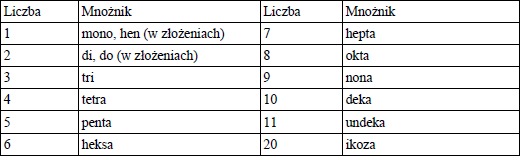
i. powyżej mnożnika 11 (undeka) kolejne powstają poprzez złożenie wyżej wymienionych, począwszy od jedności np: 14 – tetradeka, 21 – henikoza.
ii. w przypadku użycia mnożnika ikoza literę i podaje się jedynie, kiedy poprzedzająca litera jest spółgłoską np: 21 – henikoza ale 22 – dokoza
2. Lokanty
i. pozycja lokantów
lokanty są zawsze podawane bezpośrednio przed fragmentem nazwy, którego dotyczą np:

ii. pomijanie lokantów
pomijanie lokantów, jeżeli nie wprowadza niejednoznaczności, jest szeroko stosowane i dopuszczalne. Jednakże w nazwach zgodnych z nomenklaturą IUPAC dozwolone jest jedynie wtedy, jeżeli nie potrzeba wymieniać żadnego lokantu ważnego dla zdefiniowania struktury. Jeśli zachodzi potrzeba podania choćby jednego, należy podać wtedy wszystkie np: CH3CH2OH – etanol, ale Cl-CH2-CH2-OH – 2-chloroetan-1-ol. Poniżej podano szczegółowe przypadki pomijania lokantów w nazwach IUPAC:
a) pomijane są lokanty końcowe w kwasach mono i dikarboksylowych wywiedzionych z acyklicznych węglowodorów i w odpowiednich halogenkach kwasowych, amidach, nitrylach i aldehydach np: kwas butanodiowy
b) lokant 1 jest pomijany:
(a)w podstawionych związkach o jednym atomie centralnym np: chlorometan, tetrametylosilan
(b)w monopodstawionych, jednorodnych związkach o dwuatomowym łańcuchu głównym np: etanol, chlorohydrazyna
(c)w monopodstawionych, jednorodnych układach pierścieniowych np: bromobenzen, cykloheksanol
(d)w monopodstawionych układach symetrycznych, gdzie dostępny jest wyłącznie jeden rodzaj atomów wodoru, mogący ulec podstawieniu np: CH3-NH-CO-NH2 – metylomocznik
c) wszystkie lokanty są pomijane, jeżeli wszystkie możliwe pozycje są podstawione, bądź zmodyfikowane w taki sam sposób. Uwaga – przedrostek per- nie jest dłużej zalecany i nie powinien być stosowany np:

iii.zestaw najniższych lokantów
zestaw najniższych lokantów definiuje się jako zestaw, w którym, porównując kolejne lokanty w kolejności ich występowania dla różnych zestawów, dla pierwszej napotkanej różnicy występuje mniejsza wartość np: zestaw 2,3,5,8 jest niższy niż 2,4,5,6 i niższy niż 3,3,4,5. Jeżeli występują lokanty z primami – umieszczane są w kolejności za lokantami bez primów, za nimi z kolei występują lokanty z literami np: 2 jest niższe od 2′, które jest niższe od 2a, które jest niższe od 3.
Lokanty pisane dużymi literami, italikiem są niższe od lokantów pisanych alfabetem greckim, a te z kolei są niższe od lokantów zapisywanych liczbami np: N,2,3 jest niższe od 1,1,2
3. Numeracja
Kiedy w związku występuje kilka fragmentów odpowiedzialnych za ustalenie struktury, pierwszeństwo w przypisaniu zestawu najniższych lokantów dotyczy kolejno niżej wymienionych fragmentów (uszeregowane wraz ze zmniejszającym się starszeństwem):
i. ustalona numeracja układów pierścieniowych
ii. heteroatomy wstępujące bezpośrednio w łańcuchu bądź układzie pierścieniowym
iii.wskazywany atom wodoru (dotyczy głównie układów pierścieniowych) np:
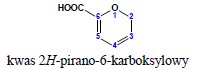
iv. główna grupa funkcyjna według starszeństwa zgodnego z punktem 10
v. nasycenie/nienasycenie układu (przedrostki hydro, dehydro, końcówki en, yn)
vi. pozostałe podstawniki nie wymienione w punkcie 10, przy czym w razie braku różnicowania wynikającego z położenia, niższe lokanty zyskują te, które są pierwsze wymieniane w nazwie np: CH3-CH(Cl)-CH(NO2)-CH3 – 2-chloro-3-nitrobutan a nie 3- chloro-2-nitrobutan
vii.jeżeli dalej pozostaje wybór, pierwszeństwo zyskują centra stereochemiczne w kolejności: Z, R
4. Porządek alfanumeryczny wymieniania podstawników
i. podstawniki proste wymieniane są zawsze w kolejności alfabetycznej niezależnie od kolejności występowania w związku. Mnożniki (di, tri itd.) są dodawane później i nie zmieniają ustalonego porządku wymieniania podstawników
ii. nazwa podstawnika złożonego zaczyna się od pierwszej litery kompletnej nazwy tego podstawnika np:
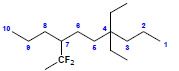
7-(1,1-difluoroetylo)-4,4-dietylodekan – kompletna nazwa podstawnika złożonego zaczyna się od litery d, więc ma on starszeństwo nad podstawnikiem prostym etylo (nazwa rozpoczyna się od litery e)
5. Elementy nazwy związku
i. Nomenklatura IUPAC w dużej mierze opiera się na tzw. nomenklaturze podstawienia, w której po wyborze podstawowego układu posiadającego odpowiednie atomy wodoru opisuje się modyfikacje jego struktury przy użyciu przedrostków i przyrostków (końcówek). Tak zbudowana nazwa ma postać:
przedrostki – układ podstawowy – końcówki – przyrostki
ii. przyrostki (punkt 10) opisują obecność podstawowej grupy funkcyjnej charakteryzującej związek (np: -ol, -on, -al). Przyrostki te są wyłączne, tzn. nie mogą być stosowane łącznie dla oznaczenia wielu grup funkcyjnych. Za pomocą przyrostka wskazuje się na najważniejszą grupę funkcyjną, pozostałe opisuje się przy użyciu odpowiedniego przedrostka np:
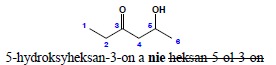
iii.końcówki -an, -en, -yn określają brak lub obecność wiązań wielokrotnych
iv. przedrostki wymieniane są w ściśle określonej kolejności. Poniżej przedstawiono stosowane przedrostki w kolejności stosowania od pozycji najbliższej do nazwy macierzystego wodorku:
a) przedrostki nierozłączne określają modyfikację układu podstawowego prowadzącą do powstania nowego układu podstawowego – należą do nich przedrostki:
(a)określające tworzenie układów pierścieniowych – cyklo, bicyklo, spiro itd
(b)określające tworzenie skoniugowanych układów pierścieniowych – benzo, furo
b) przedrostki określające wymianę atomu w układzie podstawowym na heteroatom – oksa, aza
c) wskazywane atomy wodoru zapisywane poprzez podanie lokantu i litery H pisanej italikiem
d) przedrostki hydro/dehydro określające uwodornienie układu
e) przedrostki rozłączne określające podstawienie układu podstawowego wymieniane w kolejności alfabetycznej
f) przedrostki opisujące izomerię przestrzenną
v. znaki interpunkcyjne w nazwach:
a) przecinki – oddzielają lokanty np: 2,4-dimetylocykloheksan
b) kropki – oddzielają długości połączeń w układach policyklicznych np: bicyklo[4.4.0]dekan
c) pauzy:
(a)oddzielają lokanty od słów
(b)stosowane są za nawiasami zamykającymi, jeżeli dalej następuje kolejny lokant np: 1-(chlorometylo)-4-nitrobenzen
(c)za nawiasem otwierającym pauzy nie stosuje się
(d)oddzielają przedrostki stereochemiczne od fragmentu nazwy, którego dotyczą np: (2E)-but-2-en
d) nawiasy są stosowane do:
(a)wyodrębniania nazwy podstawnika złożonego
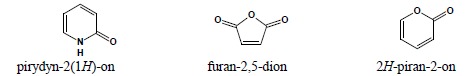
(b)wyodrębniania wskazywanych atomów wodoru oraz przedrostków opisujących aspekty stereochemiczne np: pirymidyn-2(1H)-on ale 3H-azol
(c)zagnieżdżanie nawiasów: ({[()]})
Zasady tworzenia nazw węglowodorów
6. Nazewnictwo układów podstawowych
i. związki łańcuchowe – poza nazwami metan, etan, propan i butan dalsze powstają przez dodanie do liczebnika z tabeli 1 końcówki an
ii. pierścienie monocykliczne zyskują dodatkowo przedrostek cyklo
iii.nazewnictwo układów bicyklicznych (system von Baeyera)
a) należy znaleźć główny pierścień – tj. pierścień obejmujący największą liczbę atomów
b) następnie należy znaleźć atomy przyczółkowe – są to atomy stojące na łączeniu dwóch pierścieni (łączenie główny pierścień – mostek):
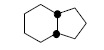
c) numeracja układu
(a)lokant 1 zyskuje jeden z atomów przyczółkowych. Począwszy od niego, numeracja podąża najdłuższą drogą po głównym pierścieniu do drugiego z atomów przyczółkowych, a następnie powraca poprzez drugi fragment głównego pierścienia
(b)następnie idąc w tym samym kierunku, numerowany jest mostek, łączący atomy przyczółkowe:
![]()
(c)kierunek numeracji powinien być tak dobrany, aby spełnił warunki przewidziane w punktach 3 ii-vii
d) wynikająca nazwa jest konstruowana w następujący sposób:
(a)w pierwszej kolejności podaje się przedrostek określający ilość pierścieni: bicyklo
(b)następnie w nawiasie kwadratowym podaje się długości dróg liczone w ilości atomów:
(1)pomiędzy atomami węzłowymi idąc od drogi najdłuższej
(2)pomiędzy atomami węzłowymi idąc drugą częścią pierścienia głownego
(3)długość mostka
(c)za nawiasem podaje się nazwę węglowodoru zawierającego tyle atomów węgla co cały układ bicykliczny
w rezultacie dla wyżej pokazanego układu powstaje nazwa:
bicyklo[4.3.1]dekan
e) przykładowe układy bicykliczne:
(a)
![]()
główny pierścień pogrubiono, układ jest bicykliczny, drogi pomiędzy atomami węzłowymi: 3 atomy, 2 atomy i 1 atom w mostku – nazwa: bicyklo[3.2.1]oktan
(b)
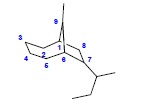
na wzorze zaznaczono poprawną numerację układu (najpierw główny pierścień, począwszy od atomu węzłowego najdłuższą drogą do drugiego atomu węzłowego, następnie druga część głównego pierścienia a na końcu mostek; kierunek numeracji dobrany tak aby podstawniki posiadały najniższy zestaw lokantów) – nazwa: 7-(butan-2-ylo)-9-metylobicyklo[4.2.1]nonan
iv. nazewnictwo układów spirocyklicznych:
monospirocykliczny węglowodór nazywa się, podając przedrostek spiro, za nim, w nawiasie kwadratowym, podaje się wielkość pierścieni, liczoną w atomach (bez wliczania łącznikowego atomu węgla) idąc od mniejszego do większego, a następnie nazwę węglowodoru równoważnego pod względem ilości atomów węgla. Numerację układu prowadzi się od pierścienia mniejszego, zaczynając od atomu sąsiadującego z łącznikowym i idąc poprzez ten pierścień do atomu łącznikowego, a następnie do drugiego pierścienia:
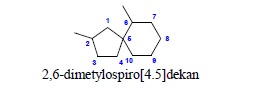
7. Tworzenie nazw podstawników
i. metoda specyficzna – od nazwy węglowodoru będącego układem macierzystym dla danego podstawnika odcina się końcówkę -an i dodaje końcówkę -yl, -yliden, -ylidyn w zależności od wartościowości grupy. Sposób ten jest ograniczony do nasyconych podstawników łańcuchowych, w których najdłuższy łańcuch węglowy rozpoczyna się w miejscu przyłączenia do układu podstawowego, bądź monopierścieniowych. W przypadku tym wolne wiązanie znajduje się zawsze na końcu łańcucha i pomija się lokant 1: CH3CH2– – etyl, CH3CH2CH(CH3)CH2CH= – 3-metylopentyliden
ii. metoda ogólna – do nazwy węglowodoru macierzystego dodaje się odpowiednią końcówkę (j.w.) z podaniem lokantu wolnego wiązania np:
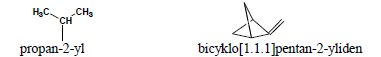
numeracja jest właściwa dla układu podstawowego podstawnika, ale tak aby wolna wartościowość miała możliwie najniższy lokant
iii.mnożniki oznaczające wielokrotne występowanie danego podstawnika w związku podaje się zgodnie z Tabelą 1 dla podstawników prostych bądź stosując mnożniki bis tris i dalej zgodnie z Tabelą 1 + przyrostek „kis” np: pentakis, dodekakis dla podstawników złożonych
8. Wybór układu podstawowego (reguły decyzyjne podane według malejącego starszeństwa):
i. posiada największą liczbę podstawników będących główną grupą funkcyjną według starszeństwa podanego w punkcie 10
ii. jest układem pierścieniowym (poniżej podano reguły wyboru podstawowego układu pierścieniowego według malejącego starszeństwa):
a) jest układem heterocyklicznym
b) posiada jak największy pierścień
c) jest układem spirocyklicznym
d) jest układem skondensowanym (np. naftalen, antracen)
e) jest układem cyklicznym zawierającym mostek (np. bicyklo[4.4.1]undekan)
f) posiada największą liczbę wiązań wielokrotnych
g) posiada największą liczbę wiązań podwójnych
h) posiada największą liczbę podstawników
iii.jest układem łańcuchowym – jeżeli jest wybór co do przeprowadzenia łańcucha głównego, następujące kryteria są brane pod uwagę (w kolejności malejącego starszeństwa):
a) zawiera największą liczbę atomów budujących szkielet łańcucha (jest najdłuższy)
b) zawiera największą liczbę wiązań wielokrotnych
c) zawiera największą liczbę wiązań podwójnych
d) zawiera większą liczbę podstawników
9. Przykłady nazw złożonych węglowodorów alifatycznych:
i.
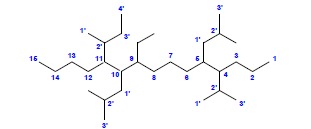
(na rysunku przedstawiono numerację łańcucha głównego, jak i podstawników – w przypadku podstawników dla przejrzystości do lokantów dodano symbol „’ ”)
Budowanie nazwy:
a) najdłuższy łańcuch węglowy – 15 at. C
b) numeracja biegnie od strony prawej (pozycje podstawników: 4,5,9,10,11, a nie: 5,6,7,11,12)
c) nazwa (podkreślono litery, które odpowiadają za kolejność występowania podstawników w nazwie): 11-(butan-2-ylo)-9-etylo-5,10-bis(2-metylopropylo)-4- (propan-2-ylo)pentadekan
ii.
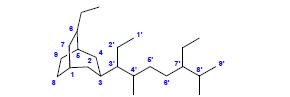
(na rysunku przedstawiono numerację łańcucha głównego, jak i podstawników – w przypadku podstawników dla przejrzystości do lokantów dodano symbol „’ ”) Budowanie nazwy:
a) układ pierścieniowy preferowany nad układ łańcuchowy w wyborze układu podstawowego (patrz wyżej)
b) układ podstawowy jest układem bicyklicznym – numeracja biegnie od atomu węzłowego najdłuższą drogą do drugiego atomu węzłowego tak aby podstawniki miały najniższe lokanty (różnicująca jest dopiero grupa etylowa!)
c) w układzie podstawnika złożonego należy znaleźć najdłuższy łańcuch połączony z układem głównym i ponumerować go tak aby miejsce przyłączenia miało najniższy lokant
d) nazwa: 6-etylo-3-(7-etylo-4,8-dimetylononan-3-ylo)bicyklo[3.2.2]nonan
10.Klasy związków (grup funkcyjnych) uszeregowane według malejącego starszeństwa dla wyboru układu podstawowego podane razem z odpowiednimi przyrostkami nazw (wybór)
i. kwasy
a) karboksylowe
-(C)OOH kwas -owy
-COOH kwas -karboksylowy
b) siarkowe:
(a) -SO2-OH kwas -sulfonowy
(b) -SO-OH kwas -sulfinowy
ii. bezwodniki
iii.estry
iv. halogenki kwasowe
v. amidy
-(C)ONH2 -amid
-CONH2 -karboksamid
vi. nitryle
-(C)N -nitryl
-CN -karbonitryl
vii.aldehydy
-(C)HO -al
-CHO -karbaldehyd
viii.ketony
>(C)O -on
>(C)S -tion
ix. hydroksy związki (alkohole i fenole traktowane są łącznie)
-OH -ol
x. aminy -NH2 -amina
11.Budowanie kompletnej nazwy związku – podsumowanie:
i. znaleźć główną grupę funkcyjną
ii. określić układ podstawowy (zawsze ten, który niesie główną grupę funkcyjną)
iii.ponumerować układ podstawowy i określić jego nazwę, dodając końcówki odpowiadające ewentualnym wiązaniom wielokrotnym i uzupełniając o końcówkę odpowiadającą głównej grupie funkcyjnej
iv. nazwać podstawniki i wymienić je w kolejności alfabetycznej
12.Przykłady:
i.
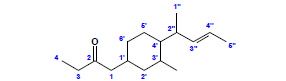
a) główna grupa funkcyjna – grupa karbonylowa (keton)
b) układ podstawowy – łańcuch węglowy, w którego przebiegu występuje grupa karbonylowa
c) nazwa wraz z końcówką – butan-2-on (numeracja przedstawiona na rysunku, prowadzona tak, aby grupa funkcyjna posiadała jak najniższy lokant)
d) w związku występuje jeden podstawnik złożony – w takim przypadku należy w pierwszej kolejności określić, co jest układem głównym podstawnika (pierścień cykloheksanu, numerowany tak, aby miejsce przyłączenia do układu podstawowego miało jak najniższy lokant) a co jego podstawnikami (grupy: metylowa i pent-3-en-2- ylowa, wymieniane w kolejności alfabetycznej)
e) nazwa całości:
1-[3-metylo-4-(pent-3-en-2-ylo)cykloheksylo]butan-2-on
ii.
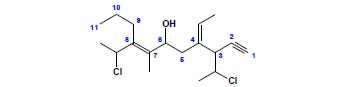
a) grupa funkcyjna – grupa hydroksylowa
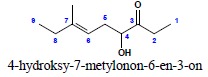
b) układ podstawowy – najdłuższy łańcuch węglowy, stojący przy grupie funkcyjnej, zawierający największą liczbę wiązań wielokrotnych. Ponieważ niezależnie od tego jak zostanie poprowadzona numeracja, grupa funkcyjna uzyska lokant 6 (taka sama odległość do obu końców układu podstawowego), numeracja prowadzona jest tak, aby wiązanie wielokrotne miało jak najniższy lokant: undec-7-en-1-yn-6-ol
c) podstawniki:
(a)grupa metylowa
(b)dwa podstawniki złożone – grupy 2-chloroetylowe
(c)grupa etylidenowa
d) nazwa związku:
3,8-bis(1-chloroetylo)-4-etylideno-7-metyloundec-7-en-1-yn-6-ol
Zasady szczegółowe
Alkeny i alkiny
1. Zasady wyboru łańcucha głównego są zachowane zgodnie z zasadami ogólnymi
2. Numeracja łańcucha głównego:
i. najniższy lokant powinno mieć dowolne wiązanie wielokrotne, niezależnie od jego rodzaju
ii. jeżeli dalej pozostaje wybór – najniższy lokant powinno posiadać wiązanie podwójne:
![]()
iii.lokanty podaje się tylko dla atomu, od którego rozpoczyna się wiązanie wielokrotne, jeżeli atom, na którym wiązanie się kończy, ma lokant o 1 większy (jak w przykładach powyżej), w przeciwnym wypadku lokant atomu kończącego wiązanie podaje się w nawiasie, bezpośrednio po lokancie oznaczającym atom rozpoczynający wiązanie:
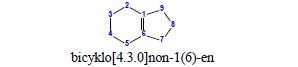
3. W nazwie zawsze podaje się najpierw końcówkę -en a dopiero po niej -yn jeśli istnieje taka potrzeba
Areny
1. W nomenklaturze systematycznej zachowano nazwy związków: benzen, toluen, ksylen, przy czym nazwy toluen i ksylen używać można wyłącznie dla związku niezmodyfikowanego.
2. Dla układów skondensowanych w nazewnictwie systematycznym zachowano nazwy (w kolejności malejącego starszeństwa):
i. piren
ii. antracen
iii.fenantren
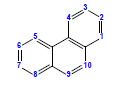
iv. fluoren (pokazano izomer 9H)
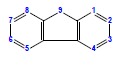
v. azulen
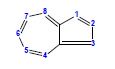
vi. naftalen
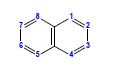
vii.inden (pokazano izomer 1H)
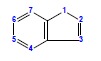
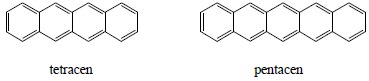
3. Układ zawierający liniowo skondensowane pierścienie benzenowe nosi nazwę: policen. Nazwa systematyczna dla konkretnych związków powstaje poprzez dodanie do liczebnika określającego ilość pierścieni końcówki cen:
Alkohole, fenole, etery i ich analogi siarkowe
1. W nazwach systematycznych zachowana zostaje jedynie nazwa: fenol
2. Nazwy systematyczne alkoholi i fenoli (obie klasy związków traktowane są identycznie) powstają poprzez dodanie do nazwy macierzystego wodorku końcówki -ol wraz z ewentualnym liczebnikiem. Końcowa litera „a” liczebnika ulega usunięciu np.: -diol, -triol ale -tetrol -pentol.
3. Wybór układu podstawowego jest zgodny z punktem 11 reguł ogólnych
4. Numeracja układu podstawowego przebiega zgodnie z punktem 3 reguł ogólnych
5. Przykłady:
i.
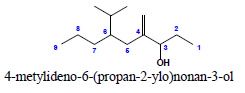
ii.
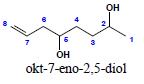
iii.
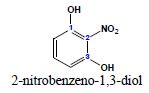
iv.
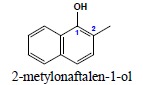
6. Przedrostka „hydroksy” używa się tylko jeżeli:
i. w związku występuje inna grupa funkcyjna o wyższym starszeństwie (zgodnie z punktem 11 reguł ogólnych)
ii. nie można użyć końcówki -ol dla oznaczenia obecności grupy OH w związku – np: we fragmencie stanowiącym podstawnik złożony:
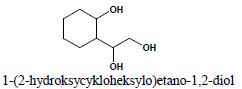
układ łańcuchowy posiada dwie grupy hydroksylowe, przez to staje się układem podstawowym
7. Siarkowe analogi zyskują końcówkę -tiol:
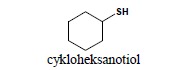
lub przedrostek sulfanylo:
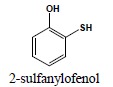
8. Etery są nazywane według dwóch metod:
i. nomenklatura podstawienia – grupa RO- jest traktowana jako podstawnik – metoda ta jest preferowana w nazewnictwie eterów
a) nazwa podstawnika RO- jest tworzona jako podstawnik złożony, składający się z nazwy podstawnika R i końcówki -oksy:
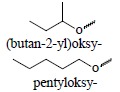
b) zachowane zostają nazwy: metoksy-, etoksy-, propoksy-, butoksy-, t-butoksy, fenoksy
c) nazwa powstaje poprzez wybranie układu podstawowego zgodnie z punktem 9 reguł ogólnych i dołączenie odpowiedniego przedrostka zgodnie z wyżej podanymi regułami:
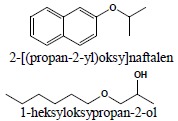
ii. „a”-nomenklatura – powstaje poprzez zastąpienie szkieletowego atomu węgla odpowiednim heteroatomem:
a) stosuje się ją dla układów:
(1)monopierścieniowych o wielkości pierścienia większej niż 10 atomów
(2)policyklicznych
(3)łańcuchowych, w których w łańcuchu głównym znajdują się co najmniej 4 heteroatomy
b) nazwa powstaje w wyniku nazwania układu podstawowego zawierającego heteroatom w taki sposób jak gdyby w miejscu tego heteroatomu znajdował się atom węgla, a następnie do tak utworzonej nazwy dodaje się przedrostek oksa wraz z lokantem określającym jego położenie. Numeracja układu dla tak tworzonej nazwy jest zgodna z punktem 3 reguł ogólnych:
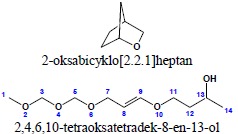
9. Siarkowe analogi eterów nazywane są analogicznie do ich tlenowych odpowiedników:
i. w nomenklaturze podstawienia dla reszty RS- jest stosowana nazwa składająca się z nazwy podstawnika R i końcówki -sulfanylo:
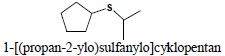
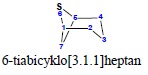
ii. w „a”-nomenklaturze obecność atomu siarki określa się przedrostkiem „tia”:
Ketony
1. Nazwy systematyczne ketonów powstają poprzez dodanie końcówki -on do nazwy macierzystego węglowodoru, poprzedzonej odpowiednim lokantem. Jeżeli w związku występuje więcej niż jedna grupa ketonowa, przed końcówką podaje się odpowiedni liczebnik. Końcowa litera „a” liczebnika ulega usunięciu (podobnie jak w przypadku alkoholi i fenoli)
2. Jeżeli w związku znajduje się ważniejsza grupa funkcyjna (według reguł starszeństwa podanych w punkcie 11) lub gdy dla oznaczenia występowania grupy ketonowej nie można użyć końcówki (np. w przypadku gdy grupa ketonowa należy do układu podstawnika) stosuje się przedrostek okso-. Uwaga: Jeżeli grupa karbonylowa występuje w pozycji 1 podstawnika łańcuchowego, podstawnik ten traktuje się jako resztę acylową (nazewnictwo reszt acylowych przedstawiono w rozdziale dotyczącym kwasów)
3. Wybór układu podstawowego jest zgodny z punktem 9 reguł ogólnych
4. Numeracja związku jest zgodna z punktem 3 reguł ogólnych
5. Przykłady i.
ii.
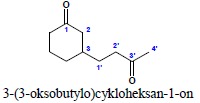
(układ pierścieniowy preferowany nad łańcuchowy, numeracja podstawnika od miejsca przyłączenia)
iii.
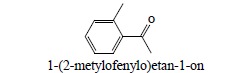
6. Chinony nazywane są zgodnie z systematycznym nazewnictwem ketonów:
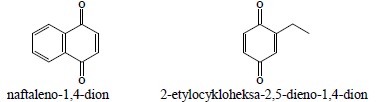
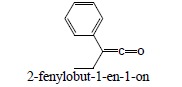
7. Keteny nazywane są zgodnie z systematycznym nazewnictwem ketonów:
i.
8. Siarkowe analogi ketonów nazywane są analogicznie jak ich tlenowe odpowiedniki i zyskują końcówkę: -tion lub przedrostek sulfanylideno-:
i.
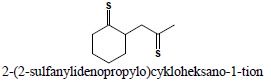
ii.
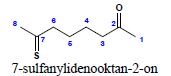
Aldehydy
1. Mono i dialdehydy łańcuchowe zyskują nazwę poprzez dodanie do nazwy węglowodoru końcówki -al (-dial)
![]()
2. Sposób numeracji, jak i sposób doboru układu podstawowego jest zgodny z odpowiednimi regułami zamieszczonymi w części ogólnej
3. Aldehydy, w których grupa CHO jest połączona z układem pierścieniowym, otrzymują końcówkę -karbaldehyd:
![]()
4. Jako nazwy systematyczne zachowane zostają nazwy: formaldehyd, acetaldehyd i benzaldehyd
5. Jeżeli w związku występuje ważniejsza grupa funkcyjna lub grupa aldehydowa występuje we fragmencie będącym układem podstawnika, zyskuje przedrostek: okso-, jeżeli znajduje się na końcu łańcucha węglowodorowego, formylo- w pozostałych przypadkach:
![]()
6. Acetale i ketale są nazywane zgodnie z nazewnictwem eterów, podobnie hemiacetale i hemiketale są nazywane jako eterowe pochodne odpowiednich alkoholi:
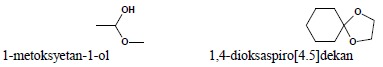
Kwasy karboksylowe
1. Mono i dikarboksylowe kwasy łańcuchowe nazywa się poprzez dodanie przed nazwą macierzystego wodorku słowa kwas i końcówki -owy ( -diowy):
![]()
2. Sposób numeracji, jak i sposób doboru układu podstawowego jest zgodny z odpowiednimi regułami zamieszczonymi w części ogólnej
3. Kwasy, w których grupa karboksylowa jest związana z układem pierścieniowym, zyskują końcówkę -karboksylowy

4. Jako preferowane nazwy IUPAC zachowane zostają nazwy: kwas mrówkowy, kwas octowy i kwas benzoesowy
5. Jeżeli grupa karboksylowa występuje jako układ podstawnika zyskuje przedrostek karboksy
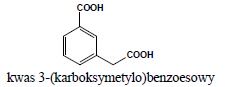
6. Grupa acylowa o postaci R-CO- zyskuje swą nazwę od odpowiedniego kwasu:
i. nazwy grup acylowych wywodzących się od kwasów, których nazwy posiadają końcówkę -owy, powstają poprzez zamianę tej końcówki na końcówkę -oil: kwas pentanowy – pentanoil, kwas 3-etylo-2-metyloheksanowy – 3-etylo-2-metyloheksanoil
ii. nazwy grup acylowych wywodzących się od kwasów, których nazwy posiadają końcówkę -karboksylowy, powstają poprzez zamianę tej końcówki na końcówkę -karbonyl: kwas cykloheksanokarboksylowy – cykloheksanokarbonyl, kwas naftaleno-2- karboksylowy – naftaleno-2-karbonyl
iii.jako preferowane nazwy IUPAC zachowane zostają nazwy grup acylowych: formyl, acetyl, benzoil
7. Nazwy halogenków kwasowych (R-CO-X) powstają poprzez podanie rodzaju atomu fluorowca (zgodnie z nazwami soli odpowiednich fluorowcowcokwasów) oraz nazwy grupy acylowej: kwas octowy – chlorek acetylu, kwas butanowy – bromek butanoilu, kwas cyklopentanokarboksylowy – chlorek cyklopentanokarbonylu
8. Nazwy bezwodników powstają poprzez zamianę słowa kwas na bezwodnik. W przypadku bezwodników niesymetrycznych podaje się nazwy obu kwasów, od których wywodzi się dany bezwodnik w kolejności alfabetycznej: kwas octowy – bezwodnik octowy, kwas cykloheksanokarboksylowy – bezwodnik cykloheksanokarboksylowy, kwas octowy i kwas pentanowy – bezwodnik octowy pentanowy
9. Nazwy bezwodników cyklicznych tworzy się według reguł nazewnictwa związków heterocyklicznych
10.Nazwy soli kwasów tworzy się poprzez zamianę końcówki -owy na -(i)an: kwas octowy – octan sodu, kwas pentanowy – pentanian potasu, kwas naftaleno-1-karboksylowy – naftaleno-1-karboksylan amonu
11.Nazwy soli łańcuchowych kwasów dikarboksylowych (kwas -diowy) zyskują końcówkę -dionian: kwas heksanodiowy – heksanodionian disodu
12.Nazwy estrów tworzy się analogicznie do nazw soli, przy czym miejsce nazwy kationu zajmuje nazwa rodnika pochodzącego od alkoholowej komponenty estru:

13.Nazwy estrów cyklicznych (laktonów) tworzy się według reguł nazewnictwa systematycznego związków heterocyklicznych
Kwasy siarkowe
1. Nazwy kwasów postaci: R-SO2H powstają poprzez dodanie do nazwy macierzystego węglowodoru końcówki -sulfinowy oraz podanie słowa kwas przed tak powstałą nazwą
2. Nazwy kwasów postaci: R-SO3H powstają poprzez dodanie do nazwy macierzystego węglowodoru końcówki -sulfonowy oraz podanie słowa kwas przed tak powstałą nazwą:
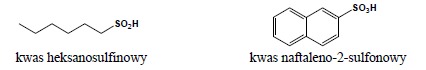
Nitryle, izocyjanki
1. Łańcuchowe nitryle zawierające jedną lub dwie grupy cyjankowe są nazywane poprzez dodanie do nazwy węglowodoru końcówki -nitryl, przy czym atom(y) węgla należące do grupy cyjankowej również są traktowane jako budujące wyjściowy węglowodór (poprzez analogię do nazewnictwa łańcuchowych kwasów karboksylowych):

2. Nitryle pierścieniowe (analogicznie do odpowiednich kwasów karboksylowych) zyskują swe nazwy poprzez dodanie do nazwy węglowodoru końcówki -karbonitryl:
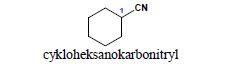
3. Zachowane, jako preferowane nazwy systematyczne, zostają nazwy nitryli wyprowadzone z zachowanych nazw systematycznych kwasów karboksylowych (kwasy octowy i benzoesowy): acetonitryl i benzonitryl
4. Jeżeli w związku występuje grupa funkcyjna o wyższym starszeństwie lub grupa cyjankowa jest fragmentem podstawnika złożonego, jej obecność wskazuje się poprzez podanie przedrostka cyjano-:
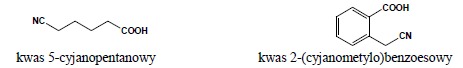
5. Związki posiadające grupę -NC są określane mianem izocyjanków. Grupa ta jest traktowana jako podstawnik prosty i określana przedrostkiem izocyjano-:

Aminy, iminy
1. Aminy są związkami będącymi formalnie podstawioną cząsteczką amoniaku typu RNH2 – aminy pierwszorzędowe, R2NH – aminy drugorzędowe i R3N – aminy trzeciorzędowe. Iminy natomiast są związkami o budowie: R-N=CR2. W rozróżnieniu starszeństwa grup funkcyjnych aminy są preferowane względem imin.
2. Aminy pierwszorzędowe:
i. Jako nazwa systematyczna zachowana zostaje jedynie: anilina z pełną możliwością podstawiania:

ii. nazwy amin pierwszorzędowych powstają poprzez dodanie do nazwy macierzystego układu końcówki -amina poprzedzonej odpowiednim lokantem. Ze względów historycznych w języku polskim pozostawiona jest litera -o- pomiędzy nazwą węglowodoru a końcówką:

iii.związki posiadające większą liczbę grup aminowych przyłączonych do układu podstawowego nazywa się analogicznie, dodając odpowiedni liczebnik przed końcówką amina. Końcowa litera „a” liczebnika ulega usunięciu: triamina, ale tetramina, a nie tetraamina:
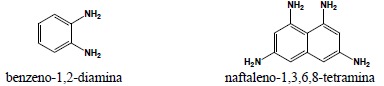
iv.w przypadku, kiedy grupa aminowa wchodzi w skład podstawnika, bądź w związku występuje ważniejsza grupa funkcyjna, obecność grupy aminowej określa się, podając przedrostek amino- poprzedzony odpowiednim lokantem:

3. Aminy drugo- i trzeciorzędowe nazywa się jako podstawione przy atomie azotu aminy pierwszorzędowe. Wybór układu podstawowego jest zgodny z punktem 9 reguł ogólnych. Podstawniki są wymieniane w kolejności alfabetycznej:
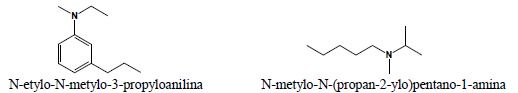
4. Jeżeli podstawiona grupa aminowa jest fragmentem podstawnika złożonego lub w związku występuje ważniejsza grupa funkcyjna – grupę taką traktuje się jako podstawnik złożony, podając reszty związane z grupą aminową w kolejności alfabetycznej, a następnie dodając przedrostek -amino-. Jeżeli z grupą aminową w takim podstawniku są związane dwie reszty, wtedy drugą, w celu uniknięcia niejednoznaczności podaje się w nawiasie:
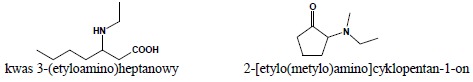
Amidy
1. Amidy są pochodnymi odpowiednich kwasów tlenowych, w których grupy OH zostały wymienione na grupy NH2.
2. Amidy kwasów, których nazwa kończy się na -owy, zyskują swoją nazwę poprzez zamianę tej końcówki na -amid: kwas propanowy – propanamid, kwas butanodiowy – butanodiamid
3. Amidy kwasów, których nazwa kończy się na -karboksylowy, zyskują nazwę poprzez wymianę tej końcówki na -karboksamid: kwas naftaleno-2-karboksylowy – naftaleno-2- karboksamid
4. Nazwy amidów pochodzących od kwasów posiadających zachowane nazwy zwyczajowe jako preferowane nazwy IUPAC: kwas octowy – acetamid, kwas benzoesowy – benzamid (amidy te mogą być podstawiane w dowolnej pozycji z zachowaniem swojej nazwy), kwas mrówkowy – formamid (amid ten może być podstawiony tylko przy atomie azotu z zachowaniem swojej nazwy)
5. Amidy pochodzące od kwasów siarkowych zyskują odpowiednie końcówki:
i. kwas sulfonowy – -sulfonamid
ii. kwas sulfinowy – -sulfinamid

6. Podstawienie amidów przy atomie (atomach) azotu jest oznaczane identycznie jak w przypadku II i III-rzędowych amin:

7. Amidy pierścieniowe są nazywane zgodnie z nomenklaturą związków heterocyklicznych.
Pochodne kwasu węglowego
1. Nazwa kwas węglowy jest zachowana jako preferowana nazwa systematyczna
i. estry i sole kwasu węglowego zyskują nazwę: węglan (np. węglan dietylu)
ii. acyl kwasu węglowego -CO- nosi nazwę: karbonyl
iii.chlorek kwasu węglowego (COCl2) nosi nazwę: dichlorek karbonylu
2. Pochodna postaci: H2N-CO-OH nosi nazwę: kwas karbamowy
i. estry i sole kwasu karbaminowego zyskują nazwę – karbaminian:
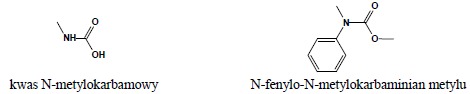
ii. acyl kwasu karbamowego (H2N-CO-) nosi nazwę: karbamoil
iii.chlorek kwasu karbaminowego (H2N-CO-Cl) nosi nazwę: chlorek karbamoilu
3. Kwas postaci Cl-COOH nosi nazwę: kwas chloromrówkowy
4. Związek będący diamidem kwasu węglowego posiada zachowaną jako preferowana nazwa systematyczna nazwę: mocznik. Siarkowy analog nosi nazwę: tiomocznik. Poniżej podano właściwą dla mocznika numerację wraz z przykładami:
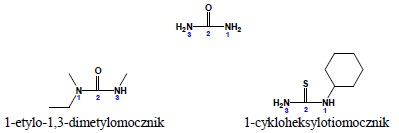
Układy heterocykliczne
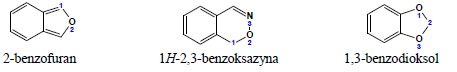
1. Zachowane jako preferowane nazwy IUPAC zostają następujące nazwy układów monopierścieniowych:
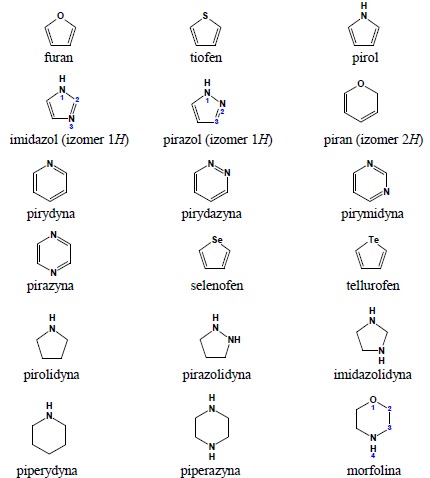
2. Układy monocykliczne zawierające od 3-10 atomów tworzących pierścień oraz przynajmniej jeden heteroatom nazywane są według rozszerzonego systemu Hantscha- Widmana. Nazwa składa się z przedrostków określających rodzaj heteroatomu (wraz z ewentualnym liczebnikami określającymi krotność wystąpienia danego atomu) oraz rdzenia określającego wielkość pierścienia i stopień jego nienasycenia
3. Poniżej podano przedrostki (wybór) określające heteroatomy w kolejności ich starszeństwa:
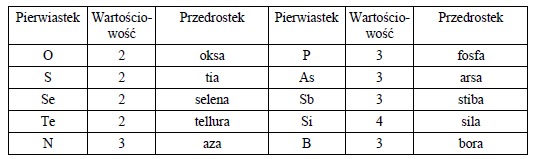
4. Poniżej podano rdzenie nazw określające wielkość i stopień nienasycenia pierścieni:
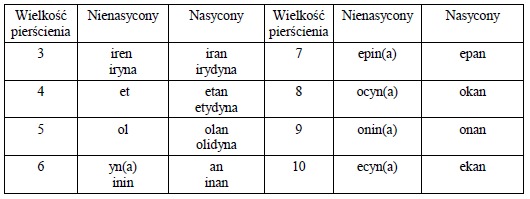
i. układ maksymalnie nienasycony jest to układ, w którym występuje maksymalna, możliwa do osiągnięcia, liczba nieskumulowanych wiązań podwójnych, wynikająca z rozmiarów pierścienia, ilości, rodzaju i sposobu występowania heteroatomów, zgodna z ich wartościowością zamieszczoną w punkcie 3
ii. układ nasycony jest to układ, w którym nie występują wiązania wielokrotne w pierścieniu
iii.dla pierścienia 3-członowego, nienasyconego rdzeń -iryna stosuje się dla pierścieni posiadających wyłącznie atom azotu jako heteroatom:
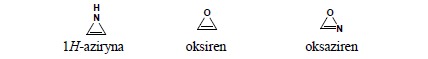
iv. dla pierścieni 3-,4- i 5-członowych rdzenie nazw: irydyna, etydyna, olidyna stosuje się dla pierścieni zawierających atom azotu (i ewentualnie oprócz niego dowolne inne):
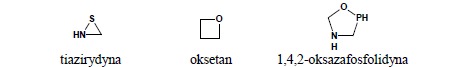
v. wybór rdzenia nazwy dla pierścieni 6-członowych zależy od rodzaju heteroatomu wymienianego na ostatniej pozycji, tuż przed rdzeniem – rdzeń inin stosuje się dla pierścieni nienasyconych, w których tym atomem jest: P, As, Sb; natomiast rdzeń inan dla pierścieni nasyconych, w których tym atomem jest: N, Si, P, As, Sb.
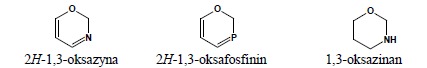
vi. ze względów historycznych, w języku polskim nazwy nienasyconych układów heterocyklicznych 6-, 7-, 8-, 9- i 10-członowych, w których atomem wymienianym na ostatniej pozycji, tuż przed rdzeniem, jest atom azotu, są rodzaju żeńskiego
5. Nazwę układu heterocyklicznego konstruuje się w niżej podany sposób
i. określić wielkość pierścienia
ii. określić nasycenie układu (układ nasycony, częściowo uwodorniony, maksymalnie nienasycony) – częściowe uwodornienie układu oznacza pojawienie się (w stosunku do układu maksymalnie nienasyconego) dwóch (lub wielokrotności dwóch) atomów nasyconych w pierścieniu (formalne przyłączenie 1 cząsteczki H2 lub wielu cząsteczek H2)
iii.znaleźć ewentualny tzw. „wskazywany atom wodoru” – występuje on w pozycji atomu pierścienia o wartościowości większej niż II a połączonego z sąsiadami wyłącznie wiązaniami pojedynczymi, niezależnie od miejsc uwodornienia
iv. dokonać numeracji układu:
a) jeżeli w związku występuje jeden heteroatom to on zyskuje lokant 1
b) jeżeli w związku występuje więcej heteroatomów tego samego rodzaju, to wtedy lokantem 1 jest zawsze oznaczony jeden z nich w taki sposób, aby wszystkie heteroatomy miały jak najniższe lokanty
c) jeżeli w związku występują różne heteroatomy, wtedy lokant 1 zyskuje atom o najwyższym starszeństwie zgodnie z tabelą przedstawioną w punkcie 3 (starszeństwo to jest zgodne z kolejnością występowania pierwiastków w układzie okresowym począwszy od grupy 17, idąc od najniższego okresu do grupy 14 do najwyższego okresu). W dalszym ciągu numerację prowadzi się w taki sposób, aby pozostałe heteroatomy miały jak najniższe lokanty, jeżeli to dalej pozostawia wybór numerację prowadzi się tak aby kolejny najniższy lokant zyskiwał heteroatom kolejny zgodnie ze starszeństwem
d) jeżeli w dalszym ciągu pozostaje wybór kierunku numeracji, prowadzi się ją tak aby najniższy lokant zyskiwały (w kolejności starszeństwa):
(1)wskazywany atom wodoru
(2)grupa funkcyjna
(3)miejsce uwodornienia układu
(4)pozostałe podstawniki
v. przedstawianie nazwy rozpoczyna się od wskazywanych atomów wodoru określanych lokantem (lokantami jeśli jest ich więcej) i dużą literą H
vi. następnie podaje się lokanty wszystkich heteroatomów występujących w pierścieniu w kolejności ich przedstawiania w nazwie a nie w kolejności wystąpienia w związku
vii.podaje się odpowiednie przedrostki odpowiadające nazwom odpowiednich heteroatomów w kolejności ich starszeństwa, poprzedzone ewentualnymi mnożnikami, w przypadku, gdy następny fragment nazwy zaczyna się od samogłoski końcowa litera a przedrostka jest usuwana
viii.na końcu podaje się rdzeń nazwy
6. Przykłady:
i.
![]()
(i) wielkość pierścienia = 5, (ii) w związku nie można wpisać żadnego wiązania podwójnego więcej więc układ nienasycony => rdzeń -ol, (iii) numeracja od atomu tlenu (najwyższe starszeństwo) w kierunku atomu fosforu (najbliższy heteroatom), (iv) wskazywanych atomów wodoru brak, (v) brak, (vi) starszeństwo atomów: O, N, P więc lokanty podać należy w kolejności: 1,4,2- (vii) podać przedrostki odpowiadające heteroatomom w kolejności starszeństwa -oksa-aza-fosfa (viii) rdzeń -ol => kompletna nazwa: 1,4,2-oksazafosfol
ii.
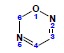
(i) wielkość pierścienia = 6, (ii) w związku nie można wpisać żadnego wiązania podwójnego więcej więc układ nienasycony => rdzeń yn, numeracja od atomu tlenu do najbliższego atomu azotu, (iv) wskazywany atom wodoru w pozycji 6 pierścienia, (v) 6H, (vi) starszeństwo atomów: O, N – lokanty 1,2,5, (vii) heteroatomy: oksa-diaz (bo dwa atomy azotu), (viii) rdzeń -yna (rodzaj żeński zgodnie z prawidłem 4.vi.) => kompletna nazwa: 6H-1,2,5-oksadiazyna
7. Częściowe uwodornienie układów nienasyconych oznacza się, podając przedrostek hydro wraz z odpowiednim lokantem. Ponieważ zawsze oznacza to usunięcie wiązania podwójnego, zastosowanie tego przedrostka wiąże się z reguły z liczebnikami di-, tetraitd. Przedrostek ten zawsze podaje się tuż przed nazwą układu, którego dotyczy, po przedrostkach określających np. obecność podstawników:
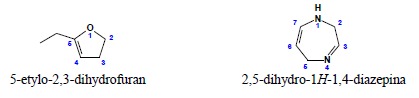
w drugim przykładzie w pierścieniu występują 3 atomy związane z sąsiednimi jedynie wiązaniami pojedynczymi, zatem jest to układ: wskazywany atom wodoru + dihydro. Ponieważ wskazywany atom wodoru, jako składnik nazwy nienasyconego układu podstawowego, posiada wyższe starszeństwo nad dodatkowe uwodornienie, to jest on wymieniany na pozycji zapewniającej najniższy lokant. Nazwa 1,2-dihydro-5H-1,4- diazepina jest zatem błędna.
8. Związki heterocykliczne posiadające przyłączoną do swej struktury grupę funkcyjną są nazywane zgodnie z nazewnictwem odpowiednich klas związków, natomiast układ heterocykliczny staje się układem podstawowym. Pamiętać należy, iż numeracja właściwa dla układów heterocyklicznych posiada wyższy priorytet nad zapewnienie najniższego lokantu dla grupy funkcyjnej, z kolei grupa funkcyjna ma wyższy priorytet nad miejscem dodatkowego uwodornienia: (patrz pkt. 5.iv)

9. Wprowadzenie podstawnika w miejsce wskazywanego atomu wodoru bądź w miejsce uwodornienia nie zwalnia z konieczności wskazywania w nazwie tych elementów pomimo, iż fizycznie, w tych pozycjach atom wodoru może już nie występować:
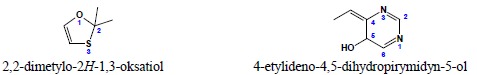
10.Prawidło 9 jest szczególnie istotne w przypadku heterocyklicznych ketonów, do których zastosowanie ma reguła 6 nazewnictwa ketonów. Należy pamiętać, iż do grupy ketonów heterocyklicznych (w sensie nazewnictwa) należą cykliczne estry, bezwodniki czy amidy
11.Nazewnictwo skondensowanych układów heterocyklicznych w głównej mierze oparte jest o system nazewnictwa skondensowanych układów aromatycznych razem dając ogólny system nazewnictwa układów skondensowanych
12.Jako nazwy systematyczne zostają zachowane (w kolejności starszeństwa idąc od najwyższego – starszeństwo to decyduje o wyborze układu podstawowego w układach skondensowanych lub układach podstawnik – układ macierzysty): akrydyna, karbazol, pterydyna, cynnolina, chinazolina, chinoksalina, naftyrydyna, ftalazyna, chinolina, izochinolina, puryna, indazol, indol, izoindol, ksanten, chromen, izochromen.
13.Zachowane również zostają (jako samodzielne układy, natomiast nie stosuje się tych nazw jako fragmentu układu skondensowanego) nazwy: fenazyna, fenoksazyna, fenotiazyna
14.Układy skondensowane składające się z pierścienia benzenowego i monopierścieniowego, co najmniej 5-członowego układu heterocyklicznego (tzw. benzoheterocykle) nazywane są poprzez podanie lokantów heteroatomów dalej słowa benzo a za nim nazwy układu heterocyklicznego. Numeracja jest prowadzona, tak aby lokant 1 należał do atomu bezpośrednio związanego z pierścieniem benzenowym, dobranego w ten sposób, aby heteroatomy posiadały jak najniższe lokanty. Jeżeli dalej pozostaje wybór, numerację dobiera się, tak aby heteroatom o wyższym starszeństwie posiadał jak najniższy lokant: