Autor: Anna Kurcek
Zawarta w komórce informacja genetyczna narażona jest na ciągłe uszkodzenia. Są one wynikiem błędów w replikacji, rekombinacji lub powstają na skutek działania czynników mutagennych – zarówno endogennych, jak i zewnętrznych. Zachowanie integralności genomu jest bardzo dla każdego organizmu, gdyż powstałe modyfikacje stanowią źródło mutacji, a ich konsekwencjami mogą być zmiany nowotworowe lub choroby genetyczne.
Komórki posiadają specjalne systemy naprawcze, które chronią genom przed utratą zawartej w nim informacji. Dzięki temu większość uszkodzeń zostaje naprawiona i nie wywołuje szkody dla organizmu. Procesy naprawy przebiegają według kilku schematów.
Naprawa DNA bezpośrednia
Polega na prostym odwróceniu powstałej zmiany z udziałem odpowiednich enzymów. Typy naprawianych uszkodzeń:
• Pęknięcia nici DNA – ligaza DNA naprawia przerwane wiązania fosfodiestrowe. Reakcja ta zwana ligacją polega na połączeniu wolnych końców z wykorzystaniem energii zgromadzonej w ATP.
• Uszkodzenie alkilacyjne DNA – metylacja lub etylacja zasad i grup fosforanowych. Reszta metylowa usuwana jest przez metylotransferazy. Białko MGMT po usunięciu grupy metylowej przenosi ją na własną cysteinę (Cys145) i ulega bezpowrotnej inaktywacji. Jest to zatem system kosztowny, zmuszający komórkę do ciągłej syntezy enzymu w dużych ilościach.
• Fotoreaktywacja – naprawianie fosfodimerów pirymidyn powstałych pod wpływem działania promieniowania UV. Katalizowana przez fotoliazę reakcja zależna jest od energii pozyskiwanej z absorpcji światła o długości fali 300–500 nm.
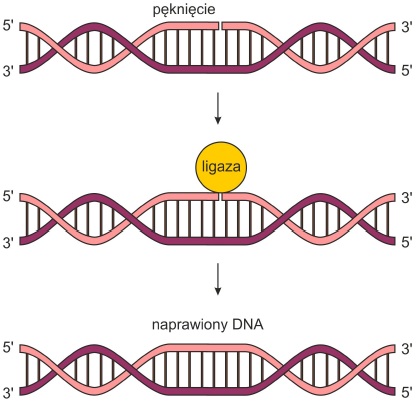
Rys. 1. Napawa pęknięcia w nici DNA
Naprawa DNA pośrednia
BER (ang. base excision repair) – koryguje niewielkie uszkodzenia poprzez wycinanie i naprawianie pojedynczych zasad, które uległy modyfikacjom chemicznym (np. alkilacji, deaminacji). Proces ten zachodzi etapowo:
• Odpowiednia glikozydaza DNA przecina wiązanie β-N-glikozydowe, a następnie usuwa uszkodzoną zasadę tworząc miejsce AP (apurynowe lub apirymidynowe).
• Endonukleaza AP rozpoznaje to miejsce i przecina wiązanie fosfodiestrowe w kierunku 5’ od powstałego uszkodzenia. W ten sposób powstają wolne końce 3’- OH.
• Wiąże się do nich polimeraza DNA I (Pol I), która następnie wypełnia lukę nową nicią syntetyzowaną na martycy DNA. U różnych organizmów w procesie tym biorą udział różne rodzaje polimerazy.
• Na koniec ligaza DNA łączy obie nici i syntetyzuje ostatnie wiązanie fosfodiestrowe.
Niektóre glikozydazy wykazują dodatkową aktywność nukleolityczną. Nacinają one łańcuch po stronie 3’ miejsca AP i tworzą jednonukleotydową lukę w DNA.
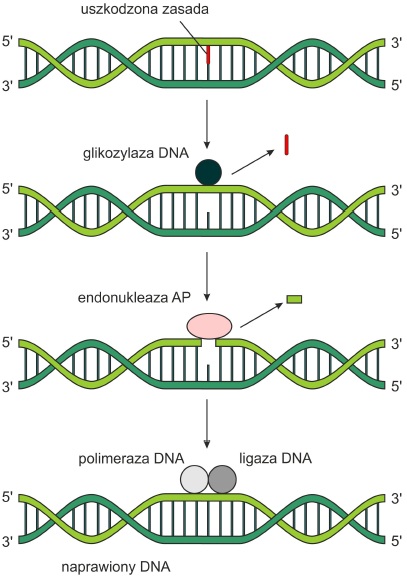
Rys. 2. Naprawa typu BER
NER (ang. nucleotide excision repair) – poprzez wycinanie uszkodzonych nukleotydów usuwa duże uszkodzenia DNA zniekształcające strukturę podwójnej helisy. Wycinany odcinek może być różnej długości.
• Białka XPA i XPC rozpoznają uszkodzenie.
• Endonukleazy XPG i XPF nacinają nić DNA po obu stronach powstałego błędu.
• Helikazy XPB XPD rozplatają podwójną helisę w sąsiedztwie uszkodzonego nukleotydu, a następnie uwalniają fragment zawierający zmianę.
• Usunięty odcinek uzupełniany jest dzięki aktywności enzymu polimerazy DNA.
• Ligazy łączą ze sobą obie nici.
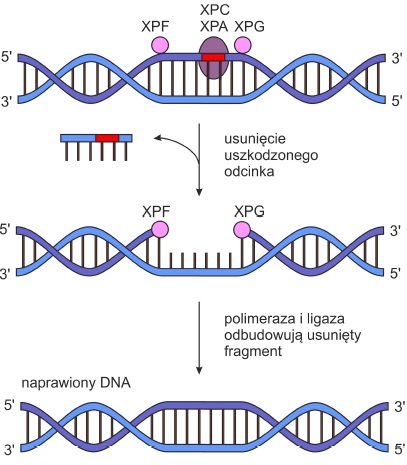
Rys. 3. Naprawa typu NER
Globalna naprawa genomu NER – GGR (ang. global genomie repair) dotyczy nici DNA nie ulegające transkrypcji i odbywa się stosunkowo wolno.
Geny podlegające aktywnej transkrypcji naprawiane są dzięki mechanizmowi NER-TCR (ang. transcription-coupled repair), a ich uszkodzenia rozpoznaje Polimeraza RNA.
Naprawa błędnie sparowanych nukleotydów
Niekomplementarne nukleotydy rozpoznawane są przez odpowiednie białka (Mut-S, Mut- H i Mut- L u Procaryota, białka kodowane przez geny hMLH i hMSH2 u Eucaryota). Identyfikacja nowo zsyntetyzowanej nici możliwa jest dzięki metyzacji oraz nieobecności połączeń między tworzącymi ją fragmentami Okazaki. Helikaza rozplata podwójną helisę, a egzonukleoaza degraduje oznaczoną nić. Jej fragment wraz z niedopasowanym nukleotydem jest usuwany i odbudowywany przez odpowiednią polimerazę DNA. Ligaza odtwarza wiązania fosfodiestrowe.
Naprawa rekombinacyjna, pozwala na naprawę uszkodzeń występujących w obu niciach (ang. double-strand breaks, DSBs). Jest ona wyjątkowo niebezpieczna dla genomu ze względu na brak matrycy umożliwiającej odtworzenie zmienionego fragmentu.
• Łączenie niehomologicznych końców (ang. non-homologous end joining, NHEJ) – system wykorzystywany do naprawy przerw w przypadku braku homologicznych sekwencji mogących posłużyć do odtworzenia ciągłości nici. Wieloskładnikowy kompleks białkowy kieruje ligazę na miejsce pęknięcia. W jego skład wchodzą: białko Ku, kinaza białkowa DNA-PKCS, białko XRCC4. Mechanizm ten nie jest dokładny, gdyż w uszkodzonym rejonie powstaje kilkunukleotydowa delecja.
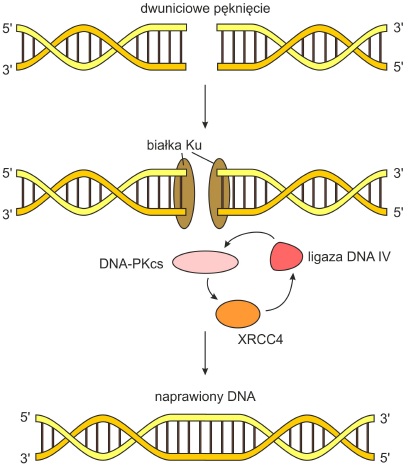
Rys. 4. Naprawa poprzez łączenie niehomologicznych końców.
• Rekombinacja homologiczna lub inaczej naprawa rekombinacyjna – polega na naprawie uszkodzonego chromosomu z wykorzystaniem siostrzanej chromatydy lub chromosomu homologicznego jako wzoru. Prowadzi do powstania jednej prawidłowej cząsteczki DNA i jednaj cząsteczki mającej dwa uszkodzone miejsca.
Naprawa indukowana, czyli system SOS (ang. save our souls) – ostateczna odpowiedź komórki bakteryjnej na rozległe uszkodzenia DNA. Jest ona regulowana przez wiele operonów i uruchamiana w przypadku pojawienia się jednoniciowego DNA (ssDNA), oligonukleotydów lub wolnych trójfosforanów nukleotydów świadczących o zahamowaniu replikacji. System SOS jest mutagenny. Obniża wierność replikacji DNA i pozostawia błędy w sekwencji nukleotydów.
Najważniejszymi regulatorami systemu SOS są białko RecA (aktywator operonów SOS) i LexA (rep resor wszystkich operonów SOS).
Gdy w komórce nie ma uszkodzeń DNA lub są one na tyle małe, że mogą być naprawione przez inne systemy, cząsteczki białka LexA wiążą się z promotorami operonów SOS hamując ekspresję genów. Łączą się także z promotorem genu RecA. Gdy w komórce pojawią się poważniejsze uszkodzenia, sygnał wysyłany przez ssDNA i ATP powoduje zmianę konformacji białka RecA, które stymuluje autoporteolizę białka LexA i indukcję systemu SOS. W momencie, gdy sygnał o uszkodzeniu DNA zanika, RecA powraca do nieaktywnej konformacji, która nie powoduje już autoprotolizy LexA.
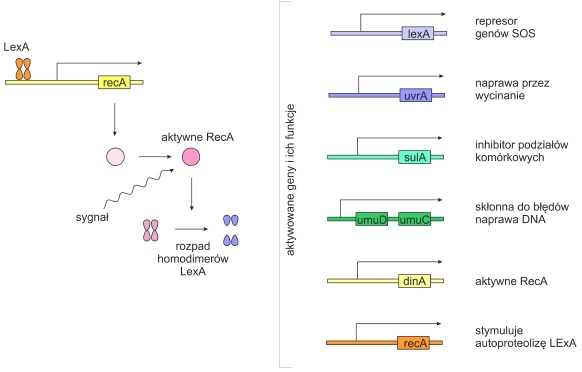
Rys. 5. Indukcja systemu SOS przez uszkodzone DNA.
Literatura:
• http://www.chemiabioorganiczna.polsl.pl/studenci/materialystudenci/6-Naprawa_DNA.pdf;
• Luiz Augusto-Pinto, Carlos Gustavo Regis da Silva, Débora de Oliveira Lopes, Alice Machado-Silva and Carlos Renato Machado „Escherichia coli as a model system to study DNA repair genes of eukaryotic organisms”; Genet. Mol. Res. 2 (1): 77-91 (2003);
• Andrzej Wierzbicki, Genetyka ogólna, wykład dla studentów II roku biotechnologii, Uniwersytet Warszawski, Wydział Biologii; http://arete.ibb.waw.pl/private/genetyka/;
• Stanisława Rogalska, Jolanta Małuszyńska, Maria J. Olszewska „Podstawy cytogenetyki roślin” Wydanie II uaktualnione; Wydawnictwo Naukowe PWN; Warszawa 2005.

