Do lat 80-tych ubiegłego wieku sądzono, że jedynie białka wykazują właściwości katalityczne. Załamanie tej teorii nastąpiło podczas badań splicingu RNA mających na celu wykrycie enzymu katalizującego wycinanie intronów RNA u orzęska Tetrahymena thermophila. Thomas Cech zauważył wtedy, że proces ten zachodzi również, gdy białka są nieobecne, co stanowiło dowód na to, że samo RNA w specyficznych sytuacjach może wykazywać właściwości enzymatyczne. Podobne wnioski wysnuł podczas równoległych badań nad dojrzewaniem tRNA w rybosomach Sidney Altman. Za to odkrycie obaj naukowcy zostali uhonorowani Nagrodą Nobla w 1989 roku w dziedzinie chemii.
Budowa rybozymów
Strukturę pierwszorzędową rybozymów stanowi jednoniciowe RNA, zbudowane z czterech rodzajów zasad nukleotydowych – adenina, guanina, cytozyna, uracyl. Mogą one łączyć się ze sobą za pomocą wiązań wodorowych, tworząc strukturę drugorzędową w postaci pętel, wybrzuszeń czy spinek. Te z kolei oddziałując między sobą tworzą strukturę trzeciorzędową. Do prawidłowego pofałdowania niezbędna jest obecność jonów dodatnich (kationów magnezowych lub sodowych), która będzie przeszkadzała elektrostatycznemu odpychaniu się ładunków ujemnych zgromadzonych na rybonukleotydach. Jedynie cząsteczki o odpowiedniej strukturze trzeciorzędowej wykazują właściwości katalityczne.
Rodzaje rybozymów
Ze względu na budowę oraz rodzaj katalizowanej reakcji rybozymy dzielimy na grupy przedstawione w Tab. 1.
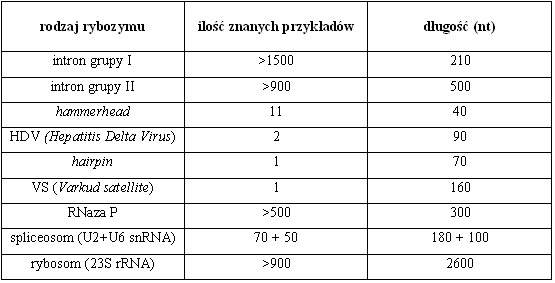
Tab. 1. Rodzaje rybozymów
Rybozymy z pierwszej grupy katalizują reakcje wycinania z nici substratu produktu, który posiada na końcu 3’ grupę hydroksylową a na końcu 5’ – fosforan. Wyróżniamy tutaj dwa typy rybozymów: introny grupy I i II. Różnią się one rodzajem cząsteczki, która dokonuje ataku na miejsce splicingowe 5’. W intronach grupy I jest nią kofaktor guanozynowy, zaś grupy II – grupa 2’-hydroksylowa reszty adenylanowej intronu. Przykładem intronu grupy I jest rybozym Tetrahymena thermophila (intron genu 26S rRNA tego orzęska). Ze względu na budowę zaliczamy go do klasy rybozymów dużych, składa się bowiem z licznych części helikalnych oraz pętli wewnętrznych. Katalizuje reakcję wycinania intronów, czyli fragmentów niekodujących własnego łańcucha RNA. Należy do rybozymów katalizujących jeden obrót reakcji, co oznacza, że traci swoje właściwości po przeprowadzeniu reakcji, bowiem następuje w nim nieodwracalna zmiana strukturalna.
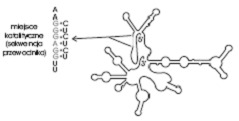
Rys. 1. Struktura drugorzędowa prekursora rRNA z Tetrahymena thermophila
Do kolejnej grupy rybozymów zaliczamy te cząstki, które katalizują reakcje prowadzące do powstania produktów o końcach 5’-hydroksylowym i cyklicznym – 2’, 3’-fosfodiestrowym. Rybozymy te różnią się między sobą strukturą centrum katalitycznego. Najczęściej spotykane to rybozymy typu „głowa młotka” (z ang. hammerhead) oraz typu „spinki” (z ang. hairpin). Rybozymy typu hairpin są rybozymami małymi i katalizują jeden obrót reakcji. Biorą udział m. in. w replikacji wirusa mozaiki tytoniowej. Podczas namnażania tworzy się łańcuch komplementarny do satelitarnego RNA, rybozym rozcina komplementarny łańcuch, liguje go tworząc matrycę do syntezy cząsteczek RNA. Rybozymy z tej grupy mogą różnić się między sobą budową. Część katalityczna jest niezmienna i zbudowana jest z dwóch heliakalnych ramion, na których znajdują się pętle wewnętrzne składające się zawsze z takich samych nukleozydów. Część nie katalityczna może zawierać różne struktury drugorzędowe.
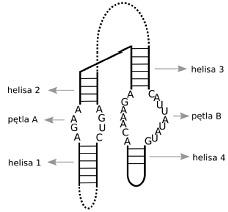
Rys 2. Budowa rybozymu typu hairpin. Linia ciągła oznacza część aktywną katalitycznie, zaś przerywana- część nie katalityczną.
Rybozymy typu hammerhead to wiroidy ulegające autokatalitycznemu splicingowi. Zbudowane są z trzech ramion odchodzących promieniście od środka składającego się z niesparowanych nukleotydów.
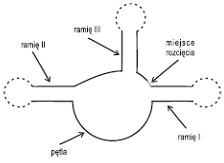
Rys. 3. Schemat budowy rybozymu typu hammerhead
RNaza P bierze udział w dojrzewaniu końca 5’ tRNA u bakterii, archeowców czy Eukariota. In vivo występuje w postaci holoenzymu (katalizę wspomaga kofaktor). U bakterii kofaktor składa się z jednej cząsteczki białka, w archeowców z czterech, zaś u organizmów eukariotycznych z dziewięciu lub dziecięciu. In vitro prezentuje swoje właściwości nawet bez udziału części białkowej. Aktywność enzymatyczną warunkuje RNA M1, rozpoznając właściwe miejsca na nici pierwotnego transkryptu.
Zastosowanie rybozymów
Rybozymy jako cząstki zdolne do enzymatycznego cięcia cząsteczek mRNA znajdują szerokie zastosowanie w terapii genowej, specyficzne cięcie mRNA może bowiem osłabiać lub zapobiegać translacji odpowiednich białek. Wykorzystuje się je w genoterapii chorób wirusowych, blokuje się w ten sposób namnażanie wirusa brodawczaka ludzkiego (human papilloma virus – HPV) czy czynnika prowadzącego do transformacji nowotworowej, w wyniku któ®ej dochodzi do powstania raka skóry, sromu i ust.
Przedstawione informacje wskazują na to, że właściwości katalityczne rybozymów wynikają ze zmian konformacyjnymi w ich strukturze trzeciorzędowej. Rybozymy mogą przeprowadzać rekacje transestryfikacji (hairpin), transferu nukleotydu (introny), hydrolizy (RNA RNazy P) czy syntezę wiązania peptydowego (rybosom). Są ważnymi pod względem biologicznym cząsteczkami, wciąż prowadzone są badania nad ich aktywnością, ponieważ:
1. rybozymy biorą udział w ważnych reakcjach, których zbadanie jest niezbędne do poznania metabolizmu komórki
2. mają one prostszą budowę niż enzymy (cztery rodzaje monomerów) oraz wykazują komplementarność pomiędzy adeniną i uracylem oraz guaniną i cytozyną, przez co mechanizm ich działania jest prostszy
3. selektywność ich działania może być wykorzystywana w terapii celowanej w RNA, choć do tego niezbędne jest poznanie stabilności chemicznej oligonukleotydów w środowisku komórkowym, transportu do wyznaczonych miejsc w komórce czy fałdowania do konformacji aktywnej
4. możliwe jest poznanie fałdowania i aktywności pojedynczych cząstek, co dostarcza informacji, które są niedostępne z powodu uśredniania towarzyszącego badaniom zespołów cząsteczek w roztworze (np. wyznaczenie stałych kinetycznych)
Autor: Karolina Podsiadły
Literatura:
1. Adamawa K., Pikuła S.: Hipotetyczna rola autokatalitycznych właściwości kwasów nukleinowych w procesie biogenezy. Kosmos Problemy Nauk Biologicznych. 2004, 53 (2): 123-131
2. Barańska M., Skrętowicz J.: Perspektywy terapii genowej. Wiadomości lekarskie 2007, 60 (7-8): 305-311
3. Hajdziona M., Molski A.: Enzymologia pojedynczych cząstek RNA: wykorzystanie techniki FRET w badaniach zwijania się i dynamiki konformacyjnej rybozymów. Wiadomości chemiczne. 2010, 64 (3-4): 173-193

